行業(yè)動(dòng)態(tài)
本土藥企、跨國藥企政策跟進(jìn)能力大
作者: 來(lái)源:神宇醫藥 日期:2015-04-21 09:25:00
醫藥網(wǎng)4月21日訊 過(guò)去4年,國內企業(yè)對“特殊審批”、“重大專(zhuān)項”和“加快品種”三大通道的跟進(jìn)度遠遠不及進(jìn)口企業(yè);但2015年第一季度,國產(chǎn)企業(yè)“特殊審批”受理號數量明顯提升。
國家無(wú)疑是鼓勵創(chuàng )新的,“重大專(zhuān)項”、“特殊審批”和“加快品種”三大通道正為創(chuàng )新藥“開(kāi)快車(chē)”。
根據咸達數據V3.1,“重大專(zhuān)項”早在2005年就有相關(guān)受理號;2004年“特殊審批”有相關(guān)受理號,但再一次有“特殊審批”標簽的受理號就到2009年了;“加快品種”的受理號是從2010年開(kāi)始的。
若統計2011~2014年三大通道的總受理號數,排名第一的是“特殊審批”,共914個(gè);其次是“重大專(zhuān)項”,共168個(gè);第三是“加快品種”,共147個(gè)(見(jiàn)圖1)。值得注意的是,2015年第一季度,咸達數據V3.1截止至2015年4月10日監測數據顯示,僅僅“特殊審批”就有相關(guān)注冊受理號80個(gè),但“加快品種”和“重大專(zhuān)項”沒(méi)有受理號數據。

三大通道政策梳理
“特殊審批”
相對于申報生產(chǎn)的第三、四項,申報臨床的第一、二項的門(mén)檻明顯更低
“特殊審批”受理號數量那么多,或許與政策有相關(guān)。
按2009年1月7日頒布的《新藥注冊特殊審批管理辦法》,享受特殊審批特殊待遇的藥品有4種情形:一是未在國內上市銷(xiāo)售的從植物、動(dòng)物、礦物等物質(zhì)中提取的有效成份及其制劑,新發(fā)現的藥材及其制劑;二是未在國內外獲準上市的化學(xué)原料藥及其制劑、生物制品;三是治療艾滋病、惡性腫瘤、罕見(jiàn)病等疾病且具有明顯臨床治療優(yōu)勢的新藥;四是治療尚無(wú)有效治療手段的疾病的新藥。其中主治病證未在國家批準的中成藥“功能主治”中收載的新藥,可以視為尚無(wú)有效治療手段的疾病的新藥。
屬于一、二項情形的,藥品注冊申請人可以在提交新藥臨床試驗申請時(shí)提出特殊審批的申請,CDE應在收到特殊審批申請后5日內進(jìn)行審查確定;屬于三、四項情形的,申請人在申報生產(chǎn)時(shí)方可提出特殊審批的申請,CDE應在收到特殊審批申請后20日內組織專(zhuān)家會(huì )議進(jìn)行審查確定。
相對于申報生產(chǎn)第三、四項,申報臨床的第一、二項的門(mén)檻明顯更低。2011~2014年,“特殊審批”申請注冊號中,申報臨床的有848個(gè)受理號,占比為92.8%,而申報生產(chǎn)的受理號僅為52個(gè),補充的有14個(gè),臨床與生產(chǎn)報批的比例達到16:1。
“重大專(zhuān)項”
主要針對10類(lèi)重大疾病,化學(xué)藥、中藥、生物藥有各自的重點(diǎn)方向
重大新藥創(chuàng )新專(zhuān)項屬于國家重大科技專(zhuān)項,一向由衛計委推動(dòng),“十二五”期間任務(wù)是研制30個(gè)創(chuàng )新藥物,改造200個(gè)左右藥物大品種。2015年的重大新藥創(chuàng )制科技重大專(zhuān)項,重點(diǎn)針對嚴重危害我國人民健康的惡性腫瘤、心腦血管疾病、神經(jīng)退行性疾病、精神性疾病、糖尿病、自身免疫性疾病、耐藥性病原菌感染、肺結核、重大病毒感染性疾病以及其他常見(jiàn)病和多發(fā)?。ê粑到y和消化系統疾病等)等10類(lèi)(種)重大疾病。
其中,化學(xué)藥主要針對神經(jīng)精神系統疾?。˙ACE、AMPA等靶點(diǎn))、代謝系統疾?。≒CSK9等靶點(diǎn))、腫瘤靶向及免疫治療(WNT、PI3K-AKT-mTOR、c-Met、PD1、PD-L1、CTLA4、miRNA等靶點(diǎn))、肺動(dòng)脈高壓及慢性阻塞性肺?。╯GC等靶點(diǎn))等新機制和新靶點(diǎn)。
中藥則重點(diǎn)支持開(kāi)展臨床優(yōu)勢突出的創(chuàng )新中藥的臨床研究(近3年內獲得臨床試驗批件,并已開(kāi)展臨床研究)。
生物藥重點(diǎn)支持新結構抗體、雙特異抗體、抗體偶聯(lián)藥物、全新結構蛋白及多肽藥物、生物類(lèi)似藥;具備新技術(shù)、新工藝制備的新型疫苗、聯(lián)合疫苗及治療疫苗等,具備較好成藥性的創(chuàng )新品種。
目前暫無(wú)相關(guān)政策發(fā)布,從CDE標記有“加快品種”的產(chǎn)品看,疫苗占較大比例
至于“加快品種”,目前暫無(wú)相關(guān)政策發(fā)布。“加快品種”的政策主要是推進(jìn)臨床亟需仿制藥優(yōu)先審評制度建設。傳說(shuō)中有62個(gè)仿制藥進(jìn)行優(yōu)先審評,但究竟是哪62個(gè)還是云里霧里。
從目前CDE標記有“加快品種”的產(chǎn)品來(lái)看,疫苗占了較大比例,如脊髓灰質(zhì)炎相關(guān)疫苗、H7N9流感病毒相關(guān)疫苗、十三價(jià)肺炎球菌疫苗、麻疹疫苗、風(fēng)疹疫苗等。
政策跟進(jìn)能力PK
進(jìn)口企業(yè)VS國內企業(yè)
三大通道吻合度:諾華NO.1,恒瑞NO.2,輝瑞NO.3
那么,“重大專(zhuān)項”、“特殊審批”和“加快品種”的注冊受理號是否都屬于國產(chǎn)廠(chǎng)家呢?
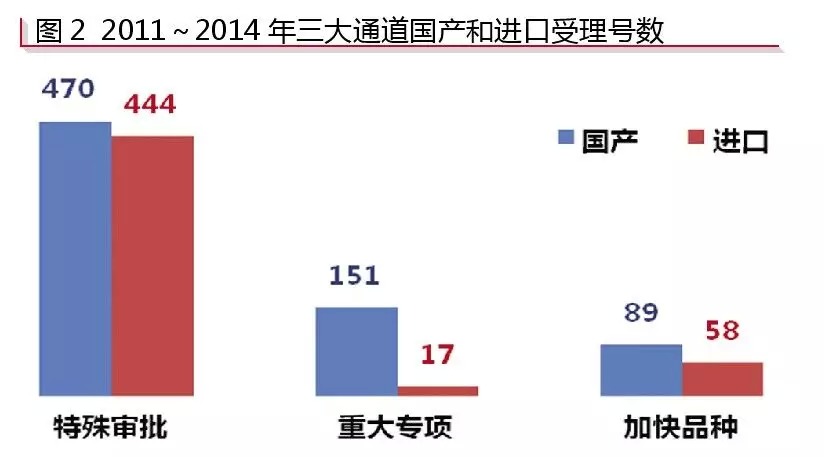
根據咸達數據V3.1的監測,“特殊審批”中,進(jìn)口藥品注冊申報的較多,占比為48.58%,共444條受理號,其中97.97%為申報臨床;“特殊審批”中,申報生產(chǎn)的國產(chǎn)受理號與進(jìn)口受理號之比約為5:1;“加快品種”中,國產(chǎn)受理號與進(jìn)口受理號之比為89:59;“重大專(zhuān)項”則更偏向于國產(chǎn)受理號,國產(chǎn)受理號與進(jìn)口受理號的比約為9:1(見(jiàn)圖2)。
一家企業(yè)如果能夠非常嫻熟地運用“重大專(zhuān)項”、“特殊審批”和“加快品種”等政策去申報注冊產(chǎn)品,雖然未必能代表其創(chuàng )新能力,但一定能說(shuō)明其非常適應國家的創(chuàng )新藥鼓勵政策。

如表1所示,三大通道受理號最多的生產(chǎn)企業(yè)是諾華,其次是恒瑞,第三位是輝瑞。前十一排名中,5個(gè)是國產(chǎn)企業(yè),6個(gè)是進(jìn)口企業(yè)。若不考慮“特殊審批”申報臨床的數據,那么排名第一的是恒瑞,其次是豪森和天壇生物,第三是拜耳。
以上數據表明,實(shí)際響應國內創(chuàng )新藥政策的國內企業(yè)并不多。相較于國內企業(yè),國外企業(yè)更積極去適應國內的新藥政策,以使自己的產(chǎn)品盡快上市。
國內企業(yè)開(kāi)始覺(jué)醒
一季度,國內企業(yè)“特殊審批”提速,是進(jìn)口企業(yè)的4倍
2011~2014年,恒瑞的受理號(除備案)共346條,屬于三大通道的受理號共63條,占整體受理號數的18.21%;豪森的受理號(除備案)共299條,屬于三大通道的受理號共63條,占整體受理號數的17.72%。
相較而言,同期科倫的受理號(除備案)共635條,但只有2個(gè)受理號屬于“特殊審批”,且申報的是臨床,尚無(wú)“重大專(zhuān)項”和“加快品種”的受理號。齊魯受理號數為448條,有8個(gè)受理號屬于“特殊審批”的臨床申請,亦無(wú)“重大專(zhuān)項”和“加快品種”的受理號??苽惖纳陥笫芾硖枖凳呛闳鸬?.8倍,但恒瑞在三大通道的受理號數是科倫的32倍。
最近傳聞,藥品審批速度要加快了,以往積壓的藥品注冊申請問(wèn)題有望3年解決。假如產(chǎn)品批文獲批速度加快,那么接下來(lái)就要開(kāi)始面對多家生產(chǎn)企業(yè)的藥品招標議價(jià)降價(jià)問(wèn)題。在一眾政策山雨欲來(lái)風(fēng)滿(mǎn)樓的層層壓力之下,國內生產(chǎn)企業(yè)越來(lái)越關(guān)注創(chuàng )新藥及其配套政策。
過(guò)去4年,國內生產(chǎn)企業(yè)實(shí)際申報的產(chǎn)品與國家三大通道政策的吻合度,遠遠不及進(jìn)口企業(yè)。國內企業(yè)申報產(chǎn)品的策略更傾向于市場(chǎng)策略,應付招標政策。
可喜的是,國內企業(yè)已認識到變革迫在眉梢。2015年第一季度,國產(chǎn)企業(yè)“特殊審批”受理號數量是進(jìn)口企業(yè)的4倍,這或許是我國創(chuàng )新藥春天到來(lái)的一個(gè)信號。
提問(wèn):
國內完全自主研發(fā)的創(chuàng )新藥有多少?
根據咸達數據V3.1,2014年1.1類(lèi)化藥9個(gè)受理號獲批生產(chǎn),涉及4個(gè)化學(xué)通用名,其中包括“阿德福韋酯”;3.1類(lèi)化藥70個(gè)受理號獲批生產(chǎn),5類(lèi)26條,6類(lèi)222條。2013年,1.1類(lèi)獲批的新藥化藥受理號有4個(gè),涉及2個(gè)化學(xué)通用名,也包括“阿德福韋酯”,還有“帕拉米韋三水合物”;同年3.1類(lèi)化藥獲批受理號95條,5類(lèi)25條,6類(lèi)223條。
若按照真正意義上的新化合物是我國自主研發(fā)才算創(chuàng )新藥,那么我國的創(chuàng )新藥和仿制藥的比例恐怕會(huì )遠低于1:100。









